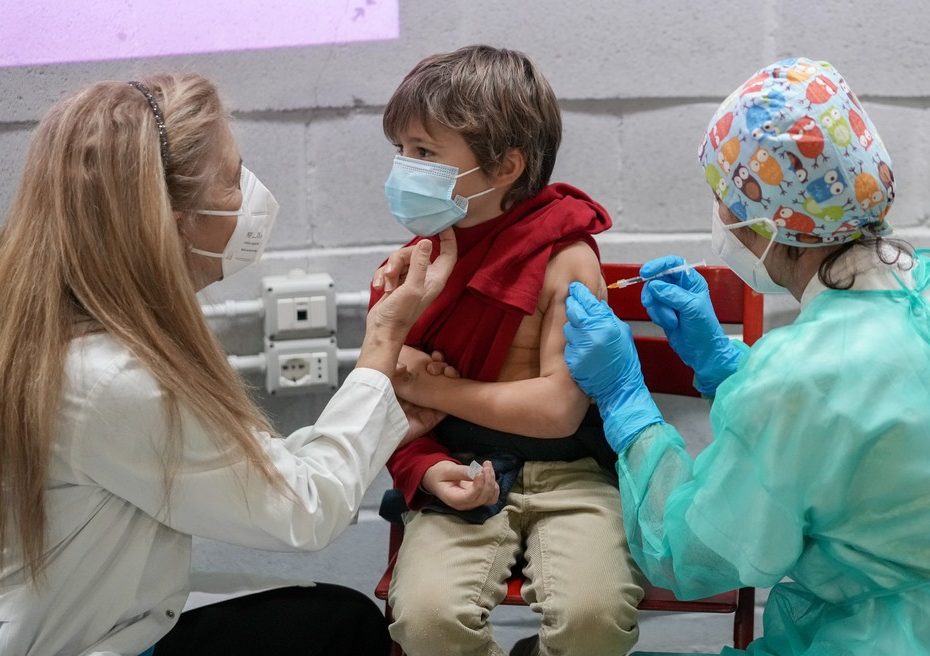
Após a Anvisa anunciar que liberou a vacinação contra Covid-19 com o imunizante da Pfizer para crianças com idades entre 5 e 11 anos, a Secretaria Estadual de Saúde Pública do Rio Grande do Norte (Sesap) estimou que a imunização desse público no estado só deve começar em janeiro de 2022, após a chegada de doses específicas.
De acordo com a coordenadora da Vigilância em Saúde, o estado tem cerca de 350 mil crianças nessa nova faixa etária a ser incluída no programa de imunização.
Ainda de acordo com ela, por se tratar do público infantil, as doses serão menores, e por isso o estado não poderia usar as vacinas já em estoque. Também é necessário esperar as orientações técnicas do Ministério da Saúde sobre o assunto.
Apesar disso, Kelly acredita que o público irá atender à convocação para a imunização.
Anvisa libera uso
Ainda não há previsão de quando a imunização vai começar porque a vacina para este público tem diferenças em relação a que foi aplicada nos adultos. Por isso, o governo federal terá que comprar uma versão específica do produto com dosagens e frascos diferentes (foto acima), apesar de o princípio ativo ser o mesmo.
A mesma autorização de uso já foi concedida pelo FDA e pela EMA (agências regulatórias de saúde dos Estados Unidos e União Europeia), além de países como Costa Rica, Colômbia, República Dominicana, Equador, El Salvador, Honduras, Panamá, Peru e Uruguai.
Versão pediátrica
A dose para as crianças entre 5 e 11 anos de idade é 1/3 da formulação já aprovada no Brasil.
A formulação pediátrica é diferente daquela aprovada anteriormente apresentada para o público com mais de 12 anos – portanto, não pode ser utilizada a formulação de adultos diluída.
A criança que completar 12 anos entre a primeira e a segunda dose deve manter a dose pediátrica.
Também participaram da avaliação especialistas das sociedades brasileiras de Infectologia (SBI), de Imunologia (SBI), de Pediatria (SBP), de Imunizações (SBIm) e de Pneumologia e Tisiologia.
Fonte: g1
